Cancer et graisses, des relations complexes
Quels sont les rapports entre la consommation de matières grasses et la survenue, puis le développement du cancer ? Deux études parues dans la revue Nature apportent de nouveaux éléments de réponse. Mais on est loin encore de recommandations nutritionnelles précises à ce sujet.
Barbara Vignaux - Publié le
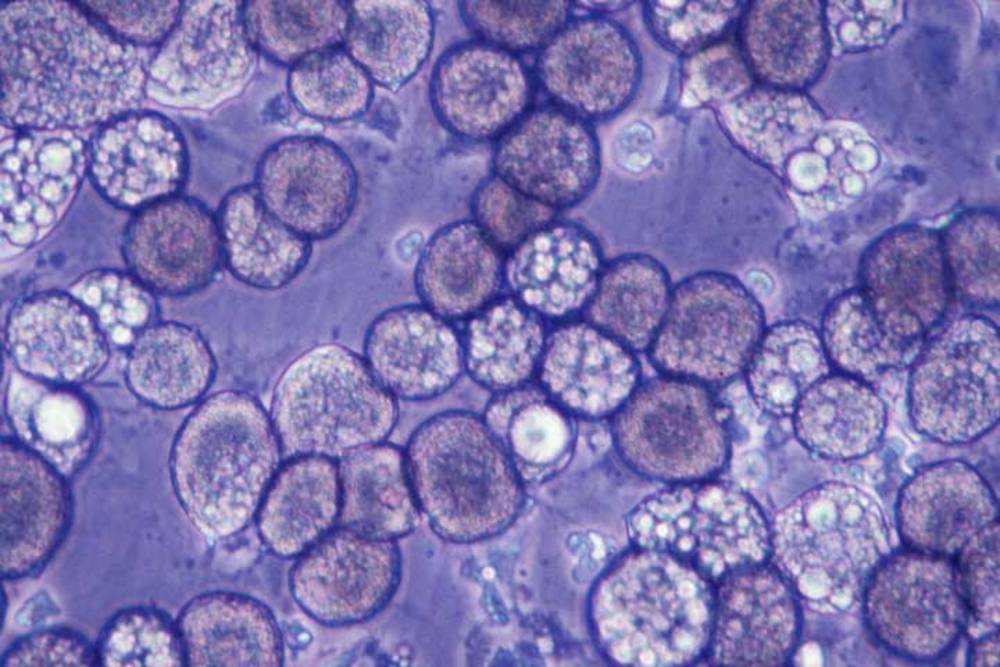
Le cancer aime les lipides et pas seulement le glucose, comme la science l’a longtemps postulé. C’est ce qu’ont montré des études menées depuis le début des années 2000. Et les recherches se poursuivent pour affiner la nature de leurs liens et la compréhension des mécanismes biologiques en cause.
Ainsi, dans un article paru en décembre dernier dans la revue Nature, des chercheurs espagnols de l’Institut de recherche en biomédecine (IRB) racontent avoir identifié « un lien direct entre la consommation d'acides gras et l’accroissement du potentiel métastatique » du cancer, c’est-à-dire à sa capacité à se disséminer dans l’organisme.
Une protéine au rôle crucial
Pour montrer l’importance des lipides dans la physiologie des cellules cancéreuses, l’équipe de l’IRB a donné une alimentation riche en graisses à des souris, avant de leur injecter des cellules tumorales d’origine humaine. Quelque 80 % des rongeurs ont développé des métastases, contre 30 % pour ceux ayant bénéficié d’une alimentation standard. Mieux : « nourries » durant deux jours à l’acide palmitique (un acide gras saturé), des cellules tumorales (cancer de la bouche) injectées à des souris ont vu leur fréquence métastasique bondir de 50 à 100 %. L’auteur principal de l’étude, Aznar Benitah, d’en conclure : « Il faut (…) maintenant comprendre cette relation intrigante entre régime alimentaire et métastases, ce d’autant plus que dans les sociétés industrielles, la consommation de graisses saturées est en forte augmentation ».
Parmi les travaux précurseurs effectués durant la décennie 2000 se trouvent ceux de Philippe Valet (Institut des maladies métaboliques et cardiovasculaires, Inserm/université Paul Sabatier) et Catherine Muller (Institut de pharmacologie et de biologie structurale, CNRS/université Paul Sabatier). Ils ont notamment montré que dans le cancer du sein, la cellule tumorale (CT) envoie des signaux aux adipocytes (ou cellules adipeuses), en charge du stockage et de la synthèse des lipides. En retour, les adipocytes nourrissent la CT par libération d’acides gras et de triglycérides (énergie stockée dans le tissu adipeux). La CT utilise les lipides ainsi stockés à la fois pour fabriquer de nouvelles membranes plasmiques et donc se reproduire, et pour libérer de l’énergie afin de se déplacer vers d’autres organes. Dans le prolongement de ces recherches, une étude parue dans Cancer Research en mai 2016 a mis en évidence, chez des sujets obèses, le rôle des exosomes, petites vésicules capables de transférer des informations d’une cellule à l’autre (en français sur le site du CNRS).
L’étude de Nature révèle notamment le rôle de la protéine CD36, en charge de la capture puis du transport des acides gras (AG) à l’intérieur des cellules tumorales. Ainsi, chez des souris atteintes de cancer de la glande mammaire, de la bouche ou de mélanome, la sur-expression de cette protéine entraîne l’apparition de métastases. Dans des tissus humains, le pouvoir métastasique de CD36 se vérifie aussi pour d’autres sites : ovaire, vessie, poumon. A contrario, l’inhibition de CD36 par injection d’anticorps réduit considérablement, voire élimine, le processus métastasique. Et ce, soulignent les auteurs, « sans effet secondaire intolérable » sur les souris. Leur objectif, désormais : « mettre au point un traitement anti-métastases ciblant CD36 ». Un pari qu’ils espèrent tenir en cinq à dix ans.
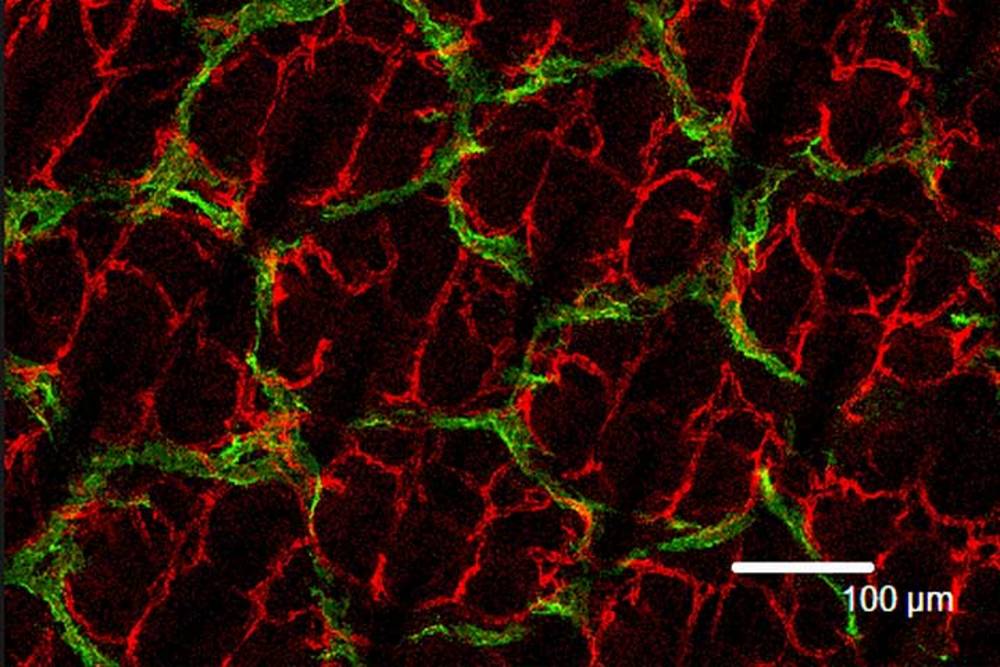
Près de 90 % des décès par cancer sont dus aux métastases, c’est-à-dire à la dissémination de la maladie dans d’autres organes que le site d’origine, par les voies sanguine ou lymphatique. L’IRB a identifié le rôle clé joué dans ce processus par la protéine CD36, qui transporte les acides gras (AG) dans les cellules, puis étudié les effets d’une modification du régime alimentaire sur le développement du cancer chez des souris. Résultat : CD36 constitue une cible thérapeutique d’avenir. © IRB 2016
Une piste anti-métastases ?
« C’est un magnifique résultat qui ouvre des perspectives thérapeutiques, commente Cédric Dray, chercheur à l’Institut des maladies métaboliques et cardiovasculaires (Inserm/Université Paul Sabatier). En effet, grâce aux anticorps dirigés contre CD36, on pourrait bloquer l’entrée de lipides dans la cellule tumorale et l’empêcher ainsi de métastaser. Mais ce faisant, tout le métabolisme de l’organisme serait perturbé car la protéine CD36 est naturellement présente dans l’organisme, et pas seulement dans les cellules tumorales. C’est un risque qu’un patient en phase terminale serait prêt à courir, mais peut-être pas un patient atteint d’un cancer peu agressif ». À moins que les chercheurs parviennent à ne cibler très précisément que les cellules tumorales ayant enclenché un programme métastasique.
Autre limite : cette protéine « ne reflète pas un type d’acide gras donné, car elle peut interagir avec tous, ajoute Véronique Chajès, chercheuse en épidémiologie nutritionnelle du Centre international de recherche contre le cancer (Circ). Donc, même si l’étude tend à montrer qu’on pourrait moduler le développement métastasique des cellules cancéreuses par les acides gras apportés par la consommation, elle ne permet pas d'établir de recommandation alimentaire ». À une échelle plus large, des études épidémiologiques permettront peut-être de préciser les acides gras avec lesquels interagit le mieux CD36 (outre l’acide palmitique).
Enfin, Cédric Dray pointe une autre menace pesant sur le patient : « On sait que la cellule tumorale (CT) est capable d’échapper à bien des contraintes pour s’adapter à un environnement changeant. Si elle parvenait à capter les lipides circulant dans le sang en "court-circuitant" CD36, rien ne freinerait plus son développement. Il faudra donc voir ce que donnent les essais cliniques sur l’anticorps CD36 ».
Acides gras, oui, mais lesquels ?
Fin décembre 2016, un nouvel acte d'accusation était dressé contre les acides gras. On savait déjà qu’ils jouaient un rôle dans l’angiogenèse, la croissance des vaisseaux sanguins au bénéfice de l'alimentation de la tumeur. Une étude parue dans Nature montre qu'ils sont aussi impliqués dans la lymphangiogenèse, c’est-à-dire la croissance des vaisseaux lymphatiques, principale voie de dissémination du cancer dans l’organisme.
Peut-on conclure de ces travaux que pour affamer la tumeur ou l’empêcher de métastaser, il faut cesser de consommer du beurre, des gâteaux et autres produits gras ? La réponse est loin d’être si simple. Unités de base des lipides, les acides gras (AG), en effet, sont présents dans de multiples sources alimentaires – produits laitiers, poissons, viandes, huiles – et remplissent de nombreuses fonctions organiques. Impossible, donc, de les supprimer de son alimentation.
Quelles graisses cibler, par conséquent ? Au Circ, Véronique Chajès cherche à cerner le rôle des AG dans la survenue d’un cancer (du sein, notamment). Elle tire dorénavant ses données d’Epic, la plus grande étude épidémiologique sur les liens entre santé et alimentation (520 000 personnes dans dix pays européens) et la première à conjuguer grande cohorte et bio-marqueurs (pour mesurer les concentrations de chaque type d’AG dans le sang).
Or des premières analyses ressortent des résultats paradoxaux : « En général, le rôle des acides gras dans la tumorigenèse est déterminant, explique Véronique Chajès. Cela a notamment été montré pour les cancers du sein, de la prostate, de l’estomac, du foie et l’adénome colorectal ». Mais les AG en cause varient selon l’organe considéré. Plus encore : « Certains inhibent la cellule cancéreuse, d’autres la stimulent ». Ainsi, la consommation d'oméga-3 n’a pas d’effet, semble-t-il, sur le risque de cancer du sein, mais est associée à une élévation du risque de cancer de la prostate et à une baisse du cancer colorectal. Les résultats sont plus clairs s'agissant de leur rôle dans l'évolution métastasique de la tumeur, puisqu'un bas taux d’oméga-3 est associé à un risque accru de dissémination et que chez les modèles animaux expérimentaux, un ajout d’oméga-3 retarde la croissance tumorale. « C’est pour cette raison qu’on attribue un rôle bénéfique aux oméga-3 : ils ralentissent la prolifération », souligne Véronique Chajès.
Les « trans » sur la sellette
Autre exemple : malgré la mauvaise réputation faite aux AG saturés, deux d’entre eux, qu’on trouve notamment dans les produits laitiers (le pentanoïque et l'heptanoïque) sont associés à une réduction du risque d'adénome colorectal, comme le montre l’analyse des données de l’étude E3N, le volet français d’Epic. Et dans les études épidémiologiques recensées par le Circ, l’acide palmitique – tant décrié – n’est pas associé à un risque cancérigène accru. Pas impossible, cela étant, qu’il le soit de manière indirecte, car le lien entre cancer et consommation d’AG mono-insaturés – fabriqués par l’organisme à partir de l’acide palmitique et des autres AG insaturés – est quant à lui avéré.
Seuls les AG « trans » industriels (utilisés comme stabilisateurs et conservateurs) peuvent faire l’objet d’un acte d’accusation sans équivoque : une teneur élevée dans le sang est associée à un risque accru de cancer du sein, montre l’analyse des données de la cohorte E3N. Certains pays européens ont d'ailleurs interdit la vente de produits qui en contiennent, dans le sillage du Danemark, dès 2003.
Véronique Chajès, du Circ, dresse le bilan des connaissances sur les liens entre acides gras et cancer.
Et à l'avenir ?
« À ce stade des recherches, il n’est donc pas possible d’émettre des recommandations nutritionnelles », conclut Véronique Chajès, en dehors d’un meilleur équilibre entre les acides gras saturés et insaturés et la réduction au minimum, voire l’élimination, des AG trans. Il faudra attendre l’analyse épidémiologique d’Epic par le Circ pour en savoir davantage. Le jeu en vaut la chandelle, puisque 40 % des cancers pourraient être évités par des modifications de nos modes de vie – tabagisme, activité sportive, alimentation…
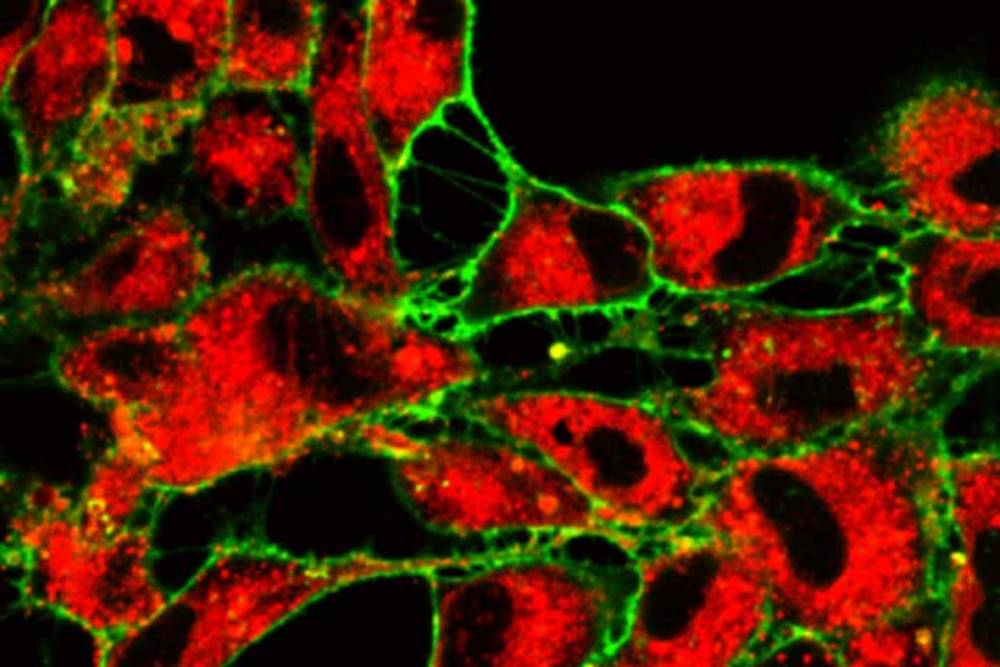
À plus long terme, de tels résultats permettront d’affiner les conseils nutritionnels donnés à la population générale, mais aussi d’améliorer les traitements. « On pourrait prélever quelques cellules de tissu tumoral, les observer, étudier leur métabolisme et dresser le profil de nutriments qu’elles utilisent afin d’en tirer des recommandations nutritionnelles précises, imagine Cédric Dray. C’est de la science-fiction aujourd’hui, mais c’est vers ce type de médecine personnalisée qu’on peut tendre. On disposerait ainsi d’un outil thérapeutique supplémentaire pour affaiblir la tumeur, sinon la tuer ».

