Le microbiote contre la malnutrition infantile
Le microbiote – c’est-à-dire la flore intestinale – est nécessaire à la croissance infantile. Mais deux études, américaine et française, montrent qu’il pourrait être aussi un allié précieux pour soigner les effets de la malnutrition.
Véronique Marsollier - Publié le
Chaque année, selon les chiffres de l'OMS et de l'UNICEF, la malnutrition est responsable de plus d’un tiers des décès chez les enfants de moins de cinq ans dans les pays en développement. Actuellement, près d’un million d’enfants en Afrique de l’Est et australe seraient atteints de malnutrition aiguë sévère en raison de la sécheresse qui touche le continent.
Le microbiote, c’est-à-dire l’ensemble des microorganismes vivant dans l’intestin, pourrait être un allié de poids pour soigner ces enfants malnutris. C’est ce que montrent deux études publiées dans le dernier numéro de Science du 19 février 2016. L’une, américaine, réalisée par l’équipe de Jeffrey Gordon du Center for Genome Sciences & Systems Biology (Saint Louis), spécialiste mondialement reconnu du microbiote, confirme le rôle des bactéries de l’intestin pour lutter contre les effets délétères de la malnutrition infantile. L’autre, française, de l’Institut de génomique fonctionnelle de Lyon, du laboratoire CarMen et de l’Unité BF2I de l’Inra (Institut national de recherche agronomique) montre les potentialités des souches d’une bactérie intestinale appartenant à l’espèce Lactobacillus plantarum.
Un microbiote altéré joue sur la croissance des enfants
L’équipe de Jeffrey Gordon travaille depuis plusieurs années sur l’apport du microbiote sur la croissance infantile. À la pointe dans ce domaine, elle avait déjà, lors de précédentes études, montré une corrélation entre les communautés microbiennes des intestins et la pathologie du syndrome de sous-nutrition aiguë qui se manifeste lors de famines sévères et impacte fortement la croissance des enfants. Les chercheurs avaient déjà remarqué que la malnutrition pouvait altérer leur microbiote. Dans cette étude, un nouveau pas est franchi. Ils démontrent que le microbiote immature est la cause de ces pathologies. Celles-ci prennent la forme de défauts de croissance, de perte de poids et de syndromes inflammatoires sévères.
L’équipe du « Gordon lab » a utilisé une méthode bien particulière. Les chercheurs ont récupéré des bactéries intestinales de nourrissons du Malawi âgés de 6 à 18 mois, sous-alimentés ou en bonne santé, en collectant leurs selles. Ils ont ensuite transplanté les échantillons à des souris dépourvues de germes intestinaux ou encore appelées axéniques.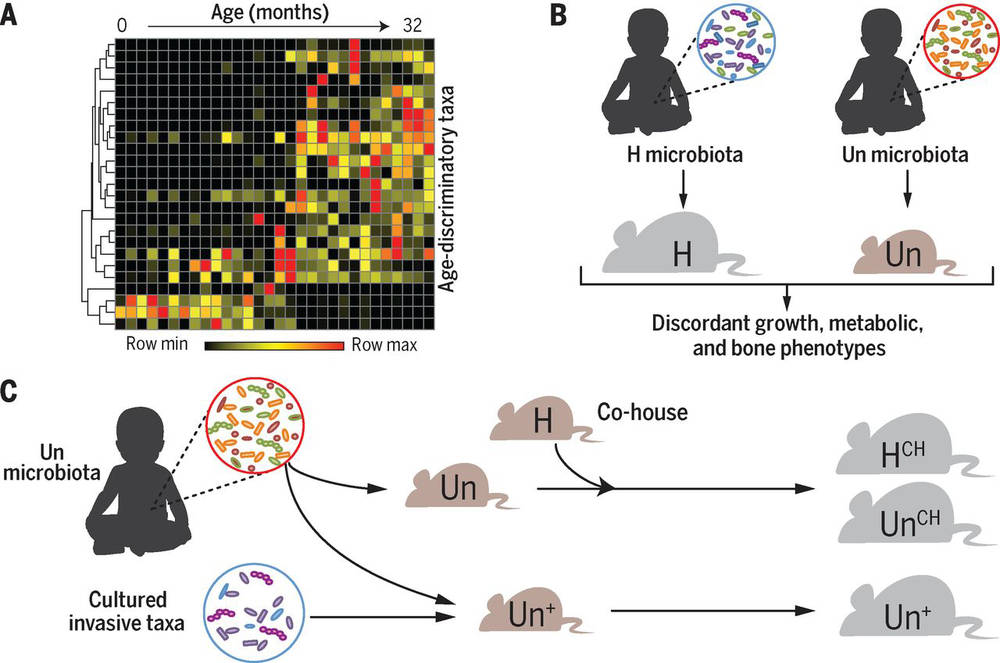
Les résultats offrent des perspectives encourageantes : les souris colonisées par le microbiote de donneurs sains ont gagné significativement plus de poids que celles à qui l’on avait implanté un microbiote d’enfants sous-alimentés. Suite à la cohabitation des souris, les chercheurs ont également constaté que le microbiote sain, en se transmettant aux souris possédant un microbiote altéré, a permis à celles-ci de retrouver une croissance normale. L’équipe de Jeffrey Gordon a pu également identifier des espèces bactériennes et certaines souches qui semblaient jouer un rôle déterminant dans l’apparition du syndrome de malnutrition aiguë ou au contraire l’en protéger. En effet, des espèces bactériennes protectrices permettraient de déclencher une résistance ou une moindre sensibilité à la sous-nutrition chez la souris.
Si cette étude n’en est qu’à un stade préclinique, elle suggère néanmoins que si l’on faisait ingérer ces souches bactériennes à des enfants souffrant de malnutrition, leur état en serait peut-être amélioré. Ils regagneraient du poids en complément avec des solutions de renutrition. Un bémol cependant : « Les espèces bactériennes isolées sont “capricieuses” donc probablement difficiles à produire à grande échelle », souligne François Leulier de l’Institut de génomique fonctionnelle de Lyon. Et ce, contrairement aux lactobacilles – bien connues – qui constituent le sujet de l’étude française réalisée par le laboratoire génomique fonctionnelle des interactions Hôtes/bactéries intestinales (Lyon) et leurs collègues...
Des lactobacilles pour lutter contre la malnutrition chronique
Ce jeune laboratoire dirigé par François Leulier a démontré, lors de précédentes études chez la drosophile, la capacité de souches bactériennes d’une espèce spécifique – en l’occurrence Lactobacillus plantarum – à favoriser la croissance juvénile en cas de sous-nutrition chronique. Restait cependant à le tester chez les mammifères, car les bactéries de leur intestin sont autrement plus diverses et complexes que celles des insectes. C’est désormais chose faite.
Dans un premier temps, les chercheurs ont comparé la croissance de souriceaux dépourvus de flore intestinale à d’autres qui en possédaient. Les chercheurs ont pu alors observer, sans surprise, une différence de prise de poids. « Il était déjà connu que le microbiote intestinal jouait sur le métabolisme et la régulation de la masse corporelle », précise François Leulier. Ce qui est nouveau, c’est que le microbiote impacte aussi la prise de taille et la croissance osseuse.

L’étape suivante a consisté à observer cet effet dans des conditions de sous-nutrition chronique. Résultat : le microbiote influence fortement la croissance des jeunes animaux ou des enfants. Les souris sans microbiote ont une croissance complètement bloquée alors que les souris porteuses d’une communauté bactérienne continuent malgré tout de grandir.
L’équipe française a ensuite étudié les effets du Lactobacillus plantarum sur les deux types de souriceaux précédemment testés. Une vraie surprise : les souriceaux, qu’ils soient nourris normalement ou sous-alimentés, regagnent du poids et de la taille tout aussi efficacement que s’ils étaient colonisés par une communauté microbienne complexe. L’effet du Lactobacillus plantarum serait donc bénéfique sur la croissance et en particulier la croissance osseuse des mammifères. « Ce qui est tout à fait novateur », se réjouit François Leulier.
Une approche complémentaire
Le chemin est encore long avant de pouvoir passer à une phase préclinique. « L’application clinique on n’y est pas. Nous sommes encore dans le concept », tempère-t-il. Dorénavant, les chercheurs souhaitent pouvoir tester ces souches de lactobacilles sur des souris sous-alimentées de façon chronique, avec un microbiote intestinal, mais dont la croissance est altérée. Si le traitement est efficace, avec une croissance qui reprend, les approches cliniques pourraient être envisagées dans le futur. Il sera alors permis d’espérer combiner des approches classiques de renutrition avec une intervention bactérienne pour soigner les enfants atteints.

