Résistance aux antibiotiques, un fléau négligé
Les bactéries résistantes aux antibiotiques progressent partout dans le monde et menacent la santé humaine. Comment lutter efficacement contre ces microbes dévastateurs ?
Textes de Marine Cygler - Publié le , mis à jour le
La médecine du 20e siècle a lutté avec succès contre les maladies bactériennes grâce aux antibiotiques. Mais aujourd’hui, de plus en plus de bactéries résistent aux médicaments qui jusque-là les éliminaient. Dans notre pays, selon Santé publique France, 12 500 décès par an sont liés à une bactérie multirésistante aux traitements. La cause principale est l’usage abusif et inapproprié des antibiotiques en médecine humaine et vétérinaire. Si l’on ne découvre pas rapidement de nouveaux antibiotiques, affirme l’Organisation mondiale de la santé (OMS), les bactéries résistantes pourraient tuer dix millions de personnes par an dans le monde en 2050. En septembre 2016, l’Assemblée générale des Nations unies a appelé les États à se mobiliser contre l’antibiorésistance et à investir dans la recherche. Quelles sont les stratégies de lutte contre ces superbactéries ? Quels antibiotiques se préparent dans les laboratoires pour demain ?
Fleming, découvreur prudent
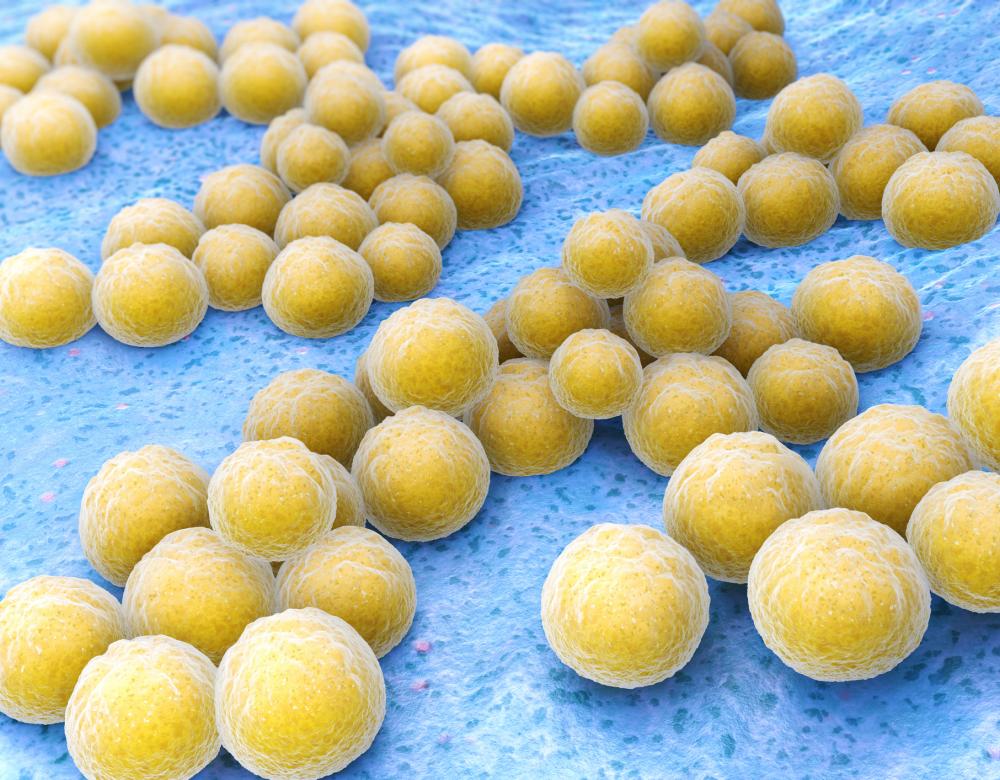
Le premier antibiotique, la pénicilline, a été découvert de façon fortuite par le biologiste écossais Alexander Fleming dans son laboratoire en 1928. Ce n’est qu’à partir des années 1940 qu’il va être exploité en médecine contre les infections causées par des bactéries. Les antibiotiques ne sont pas actifs contre les virus ou les champignons. Dès 1945, année de l’obtention de son Prix Nobel, Fleming met en garde contre le risque de développement de bactéries résistantes suite à un usage inapproprié de la pénicilline. Deux ans plus tard, les premiers cas de résistance sont observés chez des staphylocoques dorés (Staphylococcus aureus).

© David Shutterland/Getty
Un fléau de santé publique
Les bactéries résistantes représentent un coût colossal au plan humain, sanitaire et financier.
En France, 12 500 personnes en meurent chaque année. Révolution médicale du 20e siècle, les antibiotiques ont sauvé des millions de vies en traitant des maladies infectieuses auparavant incurables, comme la peste ou la tuberculose. Mais ils sont devenus aujourd’hui beaucoup moins efficaces. En effet, certaines bactéries se sont adaptées et sont désormais capables de se multiplier en présence de l’antibiotique qui auparavant les faisait disparaître ; d’autres, les plus préoccupantes, résistent même à l’action de plusieurs antibiotiques. Sur les 158 000 personnes qu’elles contaminent chaque année en France, les bactéries multirésistantes sont à l’origine de 12 500 décès (Santé publique France, étude Burden BMR, juin 2015). Soit plus de trois fois et demie le nombre de morts sur la route en 2015. 90 % des décès sont dus à des infections par les bactéries Staphylococcus aureus (staphylocoque doré) résistantes à la méticilline, Escherichia coli résistantes aux céphalosporines de troisième génération et Pseudomonas aeruginosa résistantes aux carbapénèmes (antibiotiques à large spectre). Dans le monde, selon l’OMS, l’antibiorésistance est responsable de 700 000 morts par an. Si rien n’est fait, le nombre de décès pourrait atteindre les 10 millions en 2050 et le coût de l’antibiorésistance s’élever à 100 000 milliards de dollars (91 760 milliards d’euros) (revue AMR, Rapport O’Neill, mai 2016). En effet, de nombreuses retombées, dont les coûts s’additionnent, sont à prévoir : augmentation du nombre d’hospitalisations, allongement de la durée du séjour à l’hôpital, augmentation des arrêts de travail… Avec un impact évident sur la santé des populations et l’économie mondiale.
Femmes et hommes, l'égalité en question, Insee 2017, Recherche, sciences et stéréotypes. Ipsos/La Recherche, 2017
Gare aux nouvelles ennemies !
Gare aux nouvelles ennemies ! À côté du staphylocoque doré (photo) qui reste la terreur des hôpitaux, même s’il a reculé en France de 27 % de cas de résistance à 17 % entre 2005 et 2014 (EARS-Net), d’autres bactéries résistantes apparaissent, comme certaines Escherichia coli responsables d’infections digestives et urinaires sévères et des Klebsiella pneumoniæ responsables d’infections respiratoires. Les plus dangereuses produisent une enzyme, la carbapénémase, capable de détruire une large classe d’antibiotiques, les carbapénèmes. Depuis le début des années 2000, elles sont surveillées grâce au réseau européen EARS-Net qui suit la survenue de résistances pour sept espèces de bactéries dans 29 pays.
Ut enim ad minima veniam, quis nostrum exercitationem ullam corporis suscipit laboriosam, nisi ut aliquid ex ea commodi consequatur ©Nasa
L’Homme responsable
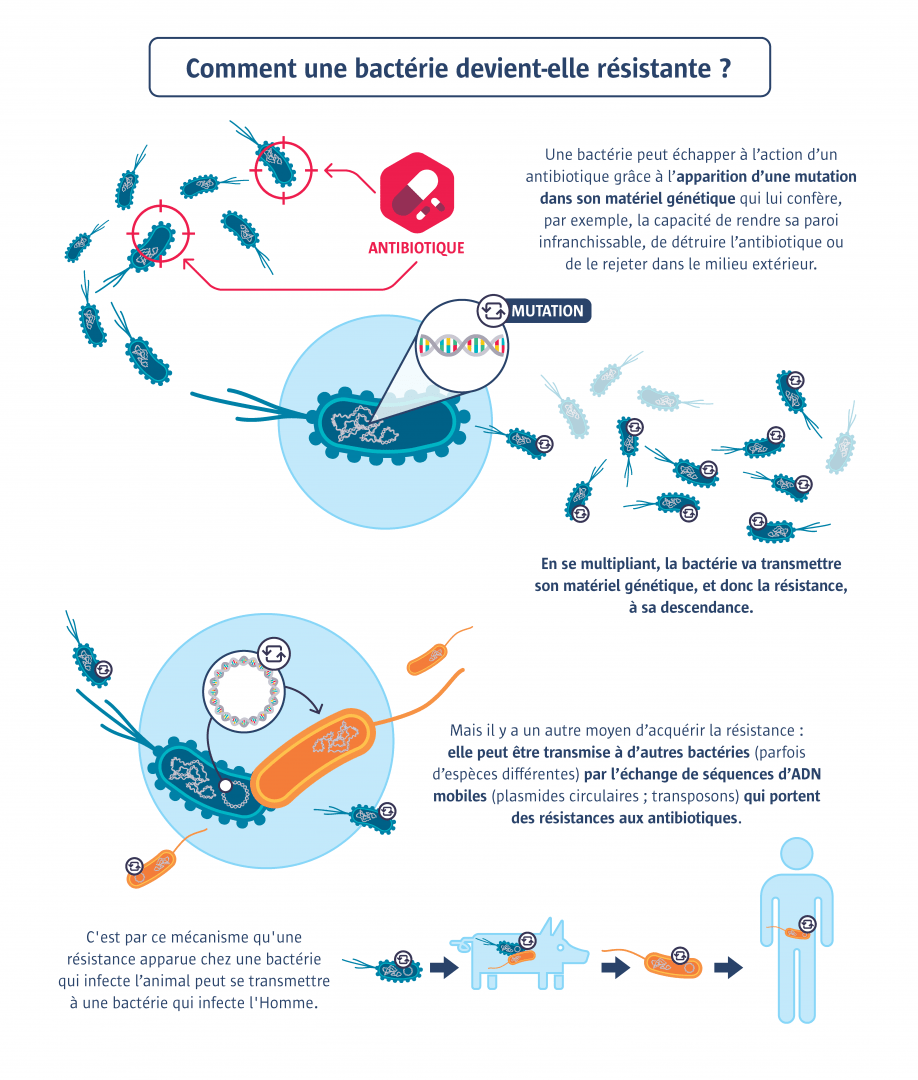
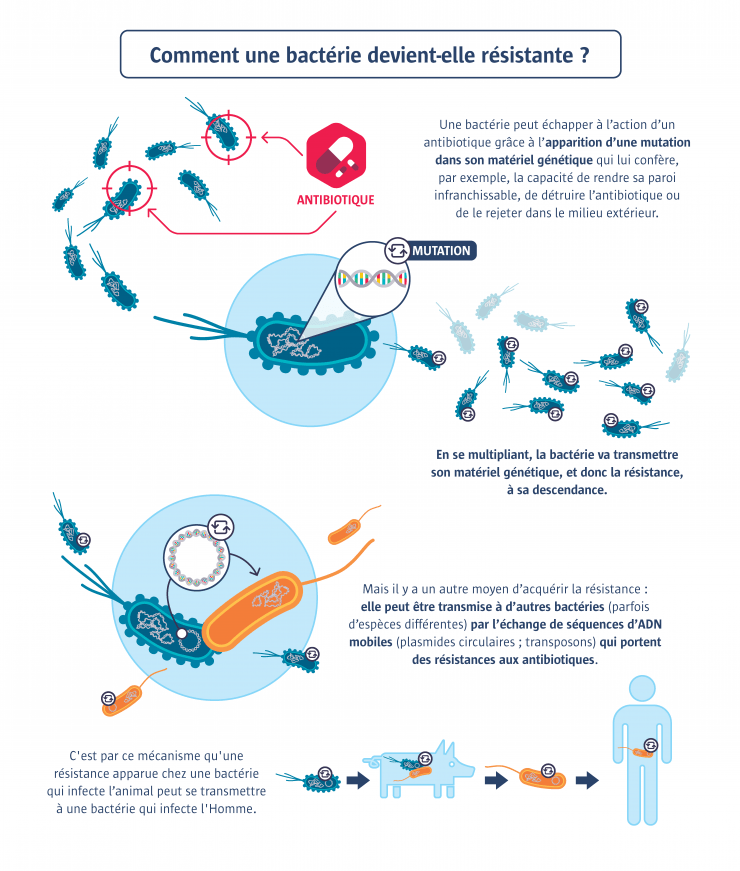
La résistance aux antibiotiques est un processus naturel de défense des bactéries. Mais trop d’antibiotiques favorise les souches résistantes.
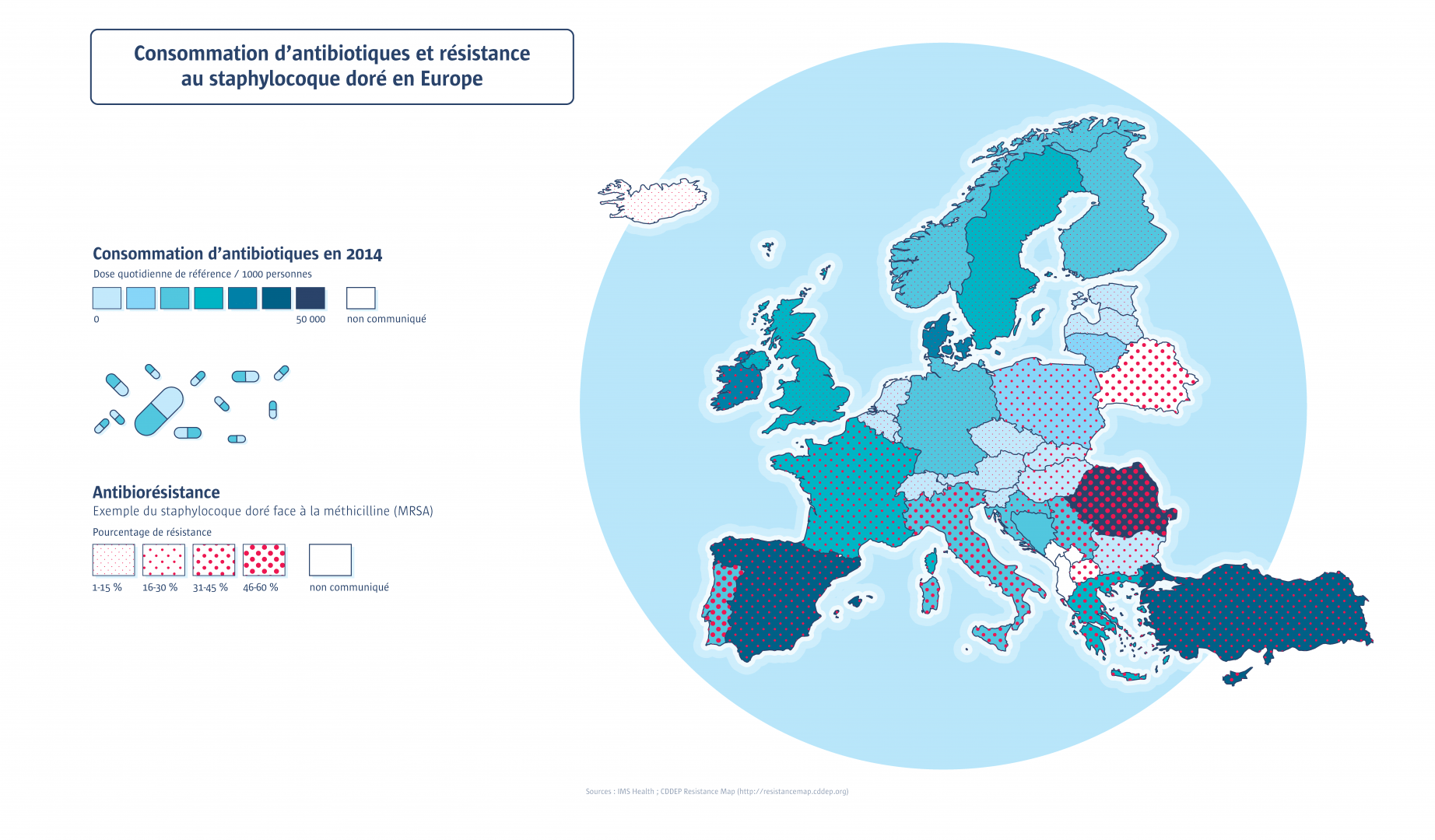
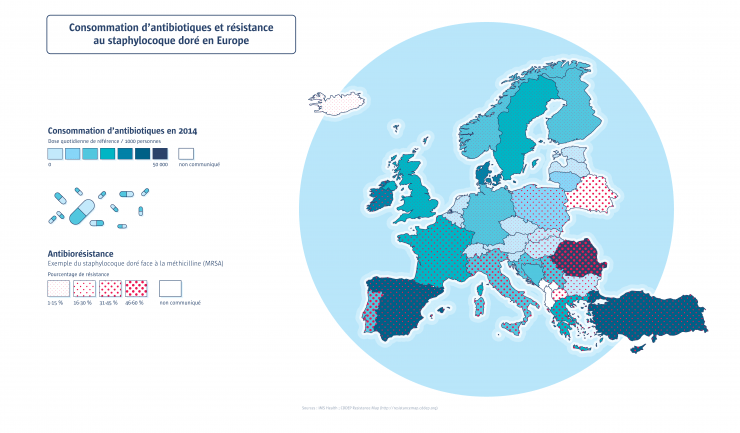
Les bactéries se sont toujours adaptées aux antibiotiques produits dans la nature. Le phénomène récent est l’accélération de ce processus d’antibiorésistance par l’utilisation massive et inappropriée d’antibiotiques en médecine humaine et vétérinaire, qui rend la lutte contre les infections bactériennes de plus en plus difficile. En effet, plus la consommation d’antibiotiques est importante, plus les résistances augmentent. Car les antibiotiques, en tuant les bactéries sensibles, sélectionnent les souches les plus coriaces (on parle de pression de sélection). Une personne infectée par une bactérie résistante peut la transmettre à son entourage, et elle va se propager. À cause des opérations chirurgicales et de la faible immunité des malades, le milieu hospitalier est le plus à risque de transmission. L’élevage, fort consommateur d’antibiotiques, contribue lui aussi au développement de bactéries résistantes et à leur propagation, y compris chez l’Homme. En mangeant de la viande, nous pouvons indirectement consommer des antibiotiques, voire des bactéries résistantes à des antibiotiques. L’administration d’avoparcine – un antibiotique utilisé comme stimulateur de croissance chez l’animal – a d’ailleurs contribué au développement de la résistance à la vancomycine (dont la structure est proche), l’un des antibiotiques les plus efficaces contre les infections à staphylocoque doré chez l’Homme. Enfin, les déplacements de populations (et donc de leurs bactéries) lors de voyages internationaux démultiplient encore les risques de propagation de ces bactéries résistantes aux antibiotiques.
Animaux aux antibios !
Selon l’Organisation mondiale de la santé, au moins 50 % des antibiotiques produits dans le monde sont destinés aux animaux d’élevage. Depuis 2006, il est interdit en Europe d’administrer des antibiotiques comme facteur de croissance dans le seul but d’augmenter la masse musculaire des animaux. Mais cette pratique perdure dans d’autres pays, comme les États-Unis ou la Chine. En outre, depuis avril 2016, en France, une cinquantaine de molécules ne peuvent plus être prescrites à titre préventif, c’est-à-dire pour protéger l’animal d’une infection potentielle.

Que font les chercheurs ?
Dans les laboratoires du monde entier, les scientifiques explorent différentes pistes pour mettre au point une nouvelle génération d’antibiotiques.
Avant d’être des produits synthétiques fabriqués à l’échelle industrielle, la plupart des antibiotiques sont des composés naturels issus de microorganismes, présents notamment dans le sol. Or plus de 90 % des bactéries trouvées dans la nature sont inexploitables car « non-cultivables » au laboratoire. L’une des pistes de recherche est donc de mettre au point de nouvelles méthodes de cultures adaptées à ces bactéries. C’est ce qui a été fait par des chercheurs américains et allemands avec la bactérie Eleftheria terrae (Nature, janvier 2015). Une approche couronnée de succès, puisqu’elle a permis aux chercheurs d’identifier une nouvelle molécule antibiotique, la teixobactine. Par ailleurs, des essais sont menés avec des peptides antimicrobiens, petites protéines aux propriétés antibiotiques produites par des animaux (grenouille, alligator, manchot…). Et des virus refont surface : les bactériophages, virus tueurs de bactéries. Utilisés en médecine humaine dès les années 1920, puis abandonnés au profit des antibiotiques, hormis en Russie et en Géorgie, les bactériophages sont de nouveau testés dans certains laboratoires et semblent prometteurs pour lutter contre l’antibiorésistance. En 2016, une équipe française a en effet montré que cette stratégie est efficace pour tuer des bactéries Escherichia coli résistantes à des antibiotiques. Enfin, les derniers outils biotechnologiques (comme Crispr-Cas9) font miroiter la possibilité future de manipuler le matériel génétique des bactéries afin d’éliminer les gènes de résistance.

Former les médecins
En France, au cours de leurs études, les futurs médecins sont de plus en plus sensibilisés au problème de la résistance aux antibiotiques. Ils apprennent comment avoir recours à ce type de médicaments pour les situations qui le nécessitent vraiment. Et en ville, dans leur cabinet, les généralistes sont incités, par exemple pour les angines, à vérifier grâce à un test qu’il s’agit bien d’une infection bactérienne et non virale (70 % des cas d’angine) pour laquelle les antibiotiques n’auront pas d’effet. Reste que dans notre pays, seuls 30 % des généralistes pratiquent ce test.
L’urgence d’une riposte mondiale
En septembre 2016, les Nations unies et son secrétaire général Ban Ki-moon tirent la sonnette d’alarme et appellent les États à se mobiliser contre l’antibiorésistance, en s’appuyant sur le plan d’action mondial élaboré par l’OMS en 2015. Pour s’attaquer à ce fléau, il faut relancer la recherche, développer de nouveaux tests de diagnostic rapides, surveiller la résistance à l’échelle mondiale, changer les pratiques d’usage des antibiotiques en médecine humaine et vétérinaire, lancer des campagnes de sensibilisation… En France, un rapport commandité par le ministère de la santé, en 2015, préconisait un plan interministériel pour lutter contre l’antibiorésistance. Un bilan de cette feuille de route a été publié en mai 2020, sous le titre Quelques mesures innovantes du plan d’action français contre l’antibiorésistance.

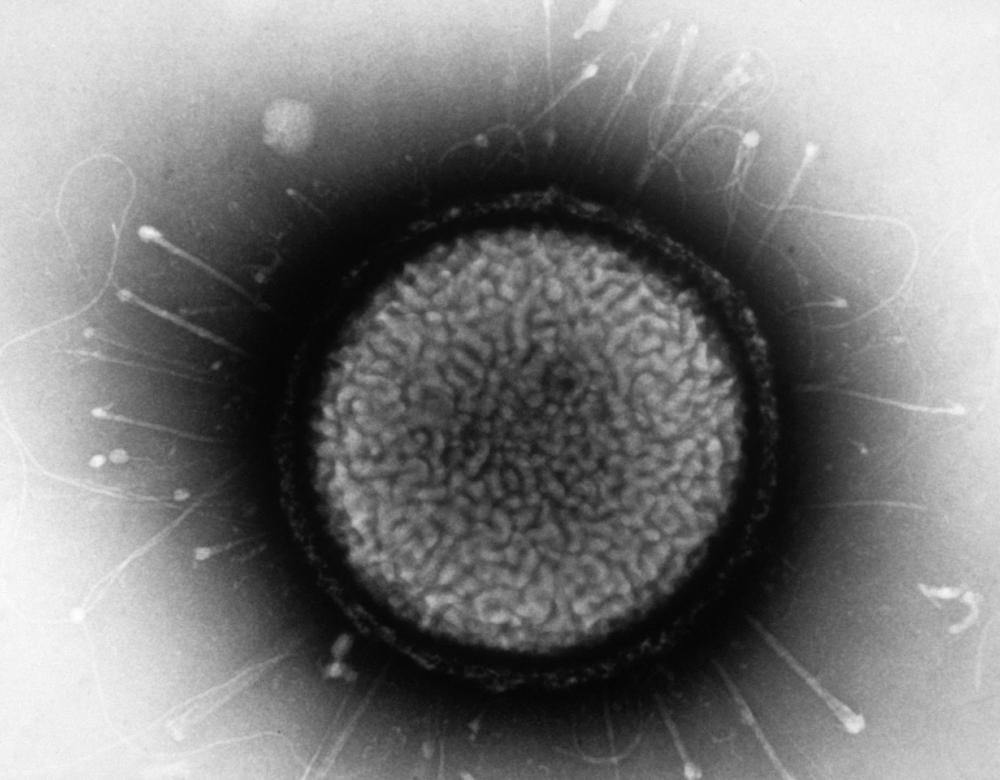
Des virus contre les bactéries
Le bactériophage est un virus qui s’attaque spécifiquement à une bactérie. Il se pose sur sa cible, transperce les parois de la bactérie grâce à un organe qui ressemble à une queue et il injecte son matériel génétique. La bactérie devient alors une fabrique à virus et finit par exploser, ce qui entraîne une dissémination des phages et surtout la mort de la bactérie. Un cocktail de bactériophages est ainsi utilisé dans le soin des plaies infectées de grands brûlés dans le cadre d’un vaste essai clinique européen.
Imiter la nature
Chez les manchots royaux de l’île de Crozet, le mâle s’occupe de l’incubation des œufs durant les dernières semaines. La femelle manchot, elle, part à la recherche de poissons. Si les poussins naissent avant le retour de leur mère, le mâle les nourrit en régurgitant le contenu de son estomac resté intact grâce à un peptide antimicrobien de la famille des défensines. Mise en évidence par des chercheurs français en 2003, cette défensine est efficace contre le staphylocoque doré et contre Aspergillus fumigatus, champignon responsable d’infections sévères comme l’aspergillose bronchopulmonaire. Aujourd’hui, selon les chercheurs, c’est le manque de financement qui freine le développement de cette molécule.


Appel à la mobilisation !
Jean Carlet, président de l’Association mondiale contre le développement des bactéries multirésistantes, nous enjoint de changer nos comportements.
In French only